
 |
|
|
Литература --> Водородные ионы в производстве обстоятельство не имеет места, то ось диска совершает вынужденное прецессионное движение, вследствие чего появляются жироскопич. Силы, влияние к-рых тем значительнее, чем больше о. Действие жироскопиче-ских сил проявляется в том, что при наличии их все явления, связанные с прогибом вала, имеют место при большей угловой скорости, чем в их отсутствии, т. е. что жироскопич. силы как бы делают вал более жестким, вследствие чего они действуют положительным образом, если угловая скорость вращения остается ниже критической. Жироскопич. силы могут возникнуть также вследствие неполного совпадения ц. т. с геометрическим центром. Лит.: 1) Классические труды по теории В.: Р о i п-S о t L., Theorie nouvelle de la rotation des corps, P., 1852; Klein F. und Sommerfeld A., €ber die Theorie des Kreisels, H. I-VI, Lpz., 1897-1910 (4 выпуска, из к-рых 4-й посвящен техническим приложениям В.); Bogaert Е. W., Leffet gyrosta-tlque et ses applications. P., 1912; Crabtree H., An Elementary Treatment of the Theory of Spinning Tops and Gyroscopic Motion, L., 1909; Perry J., Drehkreisel, ijbersetzt v. engl., Leipzig, 1904; G r a mm e 1 R., Der Kreisel, seine Theorie u. seine Anwen-dungen, Braunschweig, 1920; G e I f e r t J., Der Kreisel und seine Anwendungen, Berlin, 1927; Routh E. J., Treatise on Dynamics of a System of Rigid Bodies, London, 1905; Levi-Civita T. ed Amal-d 1 U., Lezioni di meccanica razionale, v. 2, parte П, Bologna, 1927; L о г e n z H., Technische Anwendungen d. Kreiselbewegung, Z. d. VDI*, 1919, B. 63,-p. 1224. 2) Труды, трактующие отдельные вопросы теории и технич. применений В.: а) Об опытах Фуко: Recueil des travaux scientifigues de Leon Foucault, P., 1878; Person, CR , 1852, t. 35; Trouve G., CR , 1890, t. 101; 6) 06 опытах Фёппля: F б p p 1 A., Physikal. Ztschr. , Lpz., 1914, B. 5; в) Об астатич. электрич. В.: Drexler F., Motorwagen , Berlin, 1913, В. 16; N e u b u г g e г A., Motor , В., 1919; г) О компасных В.: Anschutz Н., К а ш р f е и. S с h U 1 е г M., Jahrb. d.Schiffbautechn. Ges. , Berlin, 1909, В. 10; М a 1 g о г n G., GC , 1928, 2; д) О приборе Флерие: F а v 6 L., Revue maritime et colo-niale , Paris, 1910, v. 84; e) 06 однорельсовых ж. д.: Barkhausen G., Eisenschienenbahn und Kreisel-bahn, Z. d. VDI , 1910, B. 54, a также статьи в ♦Engineering*, L., 1907, 1910; ж) 0 В. Шлика: S с h 1 i с к С, Schiffskreisel, Jahrb. d. Schiffbautechn. Ges. , Berlin, 1909, B. 10; F б p p 1 A., Z. d. YDI , 1904,B. 48, p. 478, 1906, B. 50, p. 1032; 3) О действии жироскопич. сил в турбинах: S t о d о 1 а А., Dampf- und Gas-turbinen, 5 Aufl., Berlin, 1924; M is es R., Stabili-tat roller. Wellen, Monatshefte f. Mathem. u. Phys. , Wien, 1911, B. 22; L о r e n z H., Z.d. VDI , 1919, B. 63; S t 0 d о 1 a A., Zeltschrift f. d. ges. Turbi-nenwesen*, Mtinchen, 1918, B. 15. 3) Библиография: G г a m Ш e I R., Der Kreisel, seine Theorie und seine Anwendungen, Braunschweig, 1920; Stackel P., Element. Dynamik d. Punktsysteme, Enzykl. d. mathem. Wissenschaften*, B. 4, T. I, Art. 6, Lpz., 1901 (библ. до 1905 г.); Bogaert E. W., Leffet gyrosta-tigue (библ. до 1912 г.). P., 1912. М. Серебренников. ВОЛЬВИЛЯ ПРОЦЕСС, одно из видоизменений метода электролитич. разделения золота и серебра в сплаве Доре, содержащем от 85 до 95% золота. Применяемые для этого электролизеры готовят обычно из высших сортов фарфора, чаще всего следующих размеров: длина 406 мм, ширина 292 мм и тлу-бина 304 мм. В нек-рых случаях пользуются электролизерами и ббльших размеров-длиной 1 117 мм, шириной 609 .им и глубиной 457 мм. Электроды подвешивают на планках из фарфора, твердого каучука или стали; в случае применения больших электролизеров применяют кленовые п-ттанки, покрытые кислотоупорным лаком. Поверх планок для подводки к электродам тока располагают полосы из золота. Аноды подвешивают при помощи крючков или С-образных держалок. Размеры анодов: длина 220 мм, ши- рина 82 мм, толщина в верхи, части 12,5 мм, в нижней-9,5 мм. Ббльшая толщина анодов наверху соответствует более сильному растворению анодов в этой части. Анод погружают в электролит на глубину ~ 175 мм. Неиспользуемая часть анода, достигающая в лучшем случае 10% от его веса, возвращается в переплавку. Катодами служат прокатанные ленты из ЧИСТОГО золота, толщиной в 0,25 лш; они предварительно должны быть отожжены, так как в противном случае коробятся при электролизе. Электролитом служит раствор хлорного золота, содержащий в 1 л 50-60 г Ан, в смеси с 5-7 % свободной соляной к-ты. Электролизеры соединяются в группы по 12-15 штук, включенных последовательно. Для электролиза применяется пульсирующий или несимметрический переменный ток, получаемый от последовательно включенного генератора постоянного тока с источником переменного тока. Такой ток позволяет подвергать электролизу сплавы с более высоким содержанием серебра и применять ббльшую плотность тока при меньшем содержании в электролите свободной кислоты. В каждом электролизере помещаются три ряда анодов и четыре ряда катодов. Плотность тока на катоде варьирует от 550 до 750 А/м. Под действием тока аноды, содержащие 8-10% Ag, растворяются равномерно; золото и металлы платиновой группы переходят в раствор, а серебро, образуя нерастворимое AgCl, осаждается на дне электролизера. Кристаллы осмия не подвергаются действию тока и падают на дно электролизера. Присутствие в аноде значительных количеств серебра вызывает нарушение правильного хода электролиза, так как анод покрывается сплошным слоем AgCl, к-рое препятствует дальнейшему растворению анода, в результате чего начинает выделяться хлор. Катоды, когда вес их достигнет 4,6- 6,2 кг, вынимают, промывают на фарфоровых фильтрах, высушивают и переплавляют без всяких флюсов. Получаемые слитки золота показывают пробу 999,5-999,8, т. е. содержат 0,05-0,02% примесей. Во время электролиза происходит некоторое обеднение ванны хлорным золотом; чтобы поддержать надлежащую концентрацию его, приходится от времени до времени прибав.пять крепкого раствора AuClg. Определение содержания золота в электролите в различные стадии электролиза производят в отдельных пробах, к-рые берутся в количестве 1 см; в них золото осаждают избытком соли Мора; часть ее, не вступившая в реакцию, оттитровы-вается раствором КМПО4. Титрованный раствор соли Мора готовят растворением 154 з ее в 500 см дистиллированной воды, затем прибавляют Ъ см крепкой HgSOe и раствор доводят до 1л; 1см такого раствора осаждает 25 мг золота. Анодный шлам, содержапщй хлористое серебро, осмий и отвалившиеся частички анода, обрабатывают металлическим цинком в присутствии достаточного количества кислоты. После восстановления серебра шлам тщательно промывают на фильтре или в центрифуге и после прибавления нужного количества золота или серебра переплав- ляютв слитки, из которых далее электролизом выделяют содержащееся в них серебро. Из отработанного электролита, а также из промывных вод золото осаждают железным купоросом или медным скрапом. Т. к. выделенное этим путем золото получается в настолько мелко раздробленном виде, что дальнейшая промывка и переплавка его сопряжены с потерями, то обычно предпочитают производить выделение золота из указанных растворов электролизом. В большой электролизер помещают электролизер меньших размеров; последний заполняют крепким раствором НС1, а в большой наливают эти растворы. Сообщение между содержимым внутреннего и наружного электролизеров устанавливается при помощи серии коротких стеклянных сифонов, подвешенных на стенках внутреннего электролизера. Анод из чистого золота подвешивают во внутреннем сосуде, а во внешнем подвешивают золотые полосы, на к-рых при зймыкании цепи из указанных растворов осаждается золото. При надлежащем регулировании вольтажа выделение золота из растворов происходит нацело, В это же время во внутреннем сосуде получают крепкий раствор AuClg, к-рый затем применяют для поддержания нужной концентрации золота в растворе во время электролиза сплава. Все отработанные растворы после выделения золота и серебра собирают в деревянных чанах и из них выделяют помощью железа медь, а также последние остатки благородных металлов. В случае присутствия в отработанном электролите платиновых металлов, последние, кроме палладия, осаждают в виде малорастворимых комплексных солей насыщенным раствором хлористого аммония. После просветления раствора последний сливают с осадка и для выделения Pd подвергают электролизу; в качестве анода применяют уголь, а катодом служит золотая пластина. При электролизе такого раствора вы-деляюпщйся на аноде хлор переводит PdClg в PdCl, который и осаждается в виде комплексной соли красного цвета. Полученные осадки платиновых металлов и палладия промывают раствором NH4CI, высушивают и слабым прокаливанием переводят в металлическое состояние. Лит.: W о h Iwi 1 1 Е., Chem. а.Met. Eng. ,v.8, N. Y., 1910; L i d d e I D. M., Handbook of Non-Ferrous Metallurgy, v. 2, p. 991, N. Y., 1926; Rose Т., Metallurgy of Gold, p. 484, N. Y., 1909. Г. Ура ов. ВОЛЬТ, международная единица электр. напряжения, равная напряжению на концах проводника с сопротивлением в 1 й, через который проходит неизменяющийся ток силою в 1 А. Обозначение: V или русское в. Первоначально В. был введен для обозначения 10* единиц напряжения в электромагнитной системе CGS (абсолютный В.). В настоящее время более точные измерения показали, что один международный В. равен 1,00045 абсолютного В. Для удобства практических измерений международному В. было дано определение при помощи нормального элемента Вестона: при 20° эдс нор-ма.яьного элемента равна 1,018300 V. Однако определенный таким образом вольт несколько меньше международного и равен 1,00042 абсолютного вольта. ВОЛЬТАКС (Voltax), новый электроизоляционный материал, обладающий очень высокими изолирующими свойствами. В состав его входит тяжелый углеводород с высокой 1°пл.. В. применяется как пропитка хл.-бум. тесьмы, идущей для изоляции про-водов\ Производится в С. Ш. А. См. Изоляционные электротехнические материалы. Лит.: Ветие generale des matiferes plastiques , Paris, 1925, V. 1, p. 257. ВОЛЬТАМЕТР, прибор для измерения силы тока по его химическим действиям. По законам Фарадея для электролиза, сила тока/, проходящего через раствор соли какого-нибудь металла,равна 96,540 у = где 96,540-моэфф-т, одинаковый для всех веществ, значение к-рого вытекает из определения единицы силы тока, п-валентность вещества в данном его соединении, А-ат. в., М- масса (в мг) вещества, выделившегося на электродах. Количество вещества в мг, выделяющееся в течение 1 ск. при силе тока 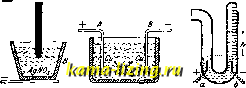 Фиг. 1. Фиг. 2. Фиг. 3. В 1 А, Т. е. при прохождении электрич. заряда в 1 С, называют электрохимич. эквивалентом этого вещества (в ф-ле обозначен буквой т). Наиболее тщательно и многократно определялся электрохимич. эквивалент серебра. На основании этих определений Международный электротехнический конгресс в Лондоне в 1908 г. принял = = 1,11800 мг, и это значение было положено в основу определения между народи. ампера. Применяются В.: медный-для измерения сильных токов, серебряный-для слабых токов при точных измерениях и газовый (иначе водяной)--в лабораторной практике. Следует упомянуть таклсе о вольтаметре свинцовом, бромовом, иодовом и ртутном. Последний употребляется иногда в качестве счетчика ампер-часов. В следующей таблице приведены значения т для различных веществ. Величины электрохимических эквивалентов.
В серебряном В. системы Кольрауша анодом слунсит серебряный массив А (фиг.1). который висит на серебряном же стерженьке, защищенном стеклянной трубочкой. Катодом служит платиновый тигель В, наполненный 15-30%-ным водным раствором нейтрального азотнокислого серебра AgNOg, получаемого перекристаллизацией продажного химически чистого AgNOg. Серебро оседает на стенках платинового тигля в виде мелкокристаллическ. осадка. Тигель перед опытом и после него взвешивают. Для того чтобы частички серебра, могущие во время электролиза отделиться от анода механически, не попали на дно тигля и не увеличивали т. о. вес осадка, на краях платинового тигля подвешен при помощи трех стеклянных крючков стеклянный защитный стаканчик, не допускающий также до катода часть электролита, близкую к аноду, в к-рой образуются кислородные соединения серебра, влияюпще на процесс. Для достаточной плотности осадка необходимо, чтобы плотность тока на катоде не превосходила 0,02 А на 1 см, а на аноде-0,2 А на 1 см. Для того чтобы перед новым взвешиванием было легче удалить осадок, не осаждают более 100 мг на 1 см катода. В серебряном В. сист. Ки-стяковского, особенно применимом для быстрого измерения слабых токов (до 0,2 А), отделившееся от анода количество серебра определяется титрованием. М е д н ы й В. состоит из двух тонких пластинок AvlB (фиг. 2), сделанных из чистой меди, а иногда одна (катод)-из платины. В качестве электролита употребляется не вполне насыщенный раствор чистого медного купороса CuSOj, иногда подкисляемый небольшим количеством HgS04. Чтобы получить плотный осадок меди на катоде, берут плотность тока на нем не более 0,04 А на 1 см. Результаты, даваемые медным В., не могут иметь большой точности по причине сравнительно малого электрохимического эквивалента меди и из-за сложных химических процессов, сопровождающих электролиз CuSO, и могущих изменить количество осажденной током меди. Для более удобного пользования медным В. катод подвешивают непосредственно к одному плечу весов. В газовом В. электролизу подвергают 10-20%-ный водный раствор H2SO4 и измеряют объем выделившегося водорода. В. состоит из U-образной стеклянной трубки с запаянным концом d (фиг. 3). В трубку запаяны два платиновых электрода а и 6. Конец трубки d градуирован на ем. При 0° и 760 мм давления 1 сж* водорода весит 0,0893 мг. Следовательно, объем водорода, выделяемый при этих условиях 1 С электричества, равен: 0,01036 0,0893 = 0,116 cjhs. Сила тока, выделившая в ск. при темп-ре t и давлении р объем водорода v см, определится из следующего выражения: 1 Н- 0,00367* 760 0,1161 где р-давление сухого водорода (без паров воды). Если Ро-показание барометра в мм ртутного столба, а h-разность уровней электролита в В., то, принимая плотность ртути почти в 12 раз больше плотности раствора H2SO4, имеем: р=р-тг- В действительности в водороде присутствуют водяные пары. Поэтому надо внести поправку f, к-рая обычно берется из таблиц. Так как водяные пары находятся над раствором поглощающей их серной кислоты, то поправку следует уменьшить. Обыкновенно вместо f берут 0,88/ . Вводя эти поправки, получают: Р = Ро- -0,88Л Лит.: Хвольсон 0. Д., Курс физики, т. 4, 5, Берлин, 1923; Эйхенвальд А. А., Электричество, 4 изд., М.-Л., 1927. Е. Нитусов. ВОЛЬТ-АМПЕР, единица электрич. мощности, равная одному ватту. Обозначение: VA или В.-а. Применяется гл. обр. как единица измерения кажущейся мощности (а также и реактивной мощности). Ничто не препятствует измерению этих мощностей в ваттах, однако измерение в В.-а. было введено гл. обр. для того, чтобы в самом названии единицы измерения показать, что дело идет не о реально потребляемой мощности, а о расчетной величине, равной произведению из напряжения на силу тока, и чтобы избежать при обозначении реактивной мощности такого, например, выражения: безваттная мощность в 150 W . В настоящее время слово безваттный заменяется словом реактивный , но измерение в В.-а, повсеместно распространено. Обоснованность применения этой единицы. измерения в настоящее время надо признать спорной. Лит.: Ермаков В. Д., Основы электрометрии, ч. I, М.-Л., 1927; G г и Ь п К., Elektrotechni-sche Messinstrumente, Berlin, 1923. ВОЛЬТМЕТР, прибор для измерения электрического напряжения между двумя точками электрической цепи, представляющий собою по большей части миллиамперметр (сш. Амперметр), последовательно соединенный с добавочным сопротивлением. Пока сопротивление такой цепи не меняется, напряжение на концах ее, по закону Ома, будет пропорционально току, проходящему через миллиамперметр, к-рый поэтому может быть градуирован прямо в вольтах. Для того чтобы общее сопротивление цепи вольтметра не изменялось от нагревания его обмотки или от изменения t° среды, добавочное сопротивление рассчитывают так, что в нем поглощается ббльшая часть всего измеряемого напряжения, и выполняют это сопротивление из материала с ничтожным Г-ным коэффициентом. Различают: 1)В. с подвижной катушкой и постоянным магнитом (фиг. 1); эти В. пригодны только для постоянного тока и имеют равномерную шкалу, так как вращающий момент М= ki-a = k.H-i = кН-Е=к-Е,  Фиг. 1
|