
 |
|
|
Литература --> Водородные ионы в производстве механических свойств от условий нагрева и охлаждения для Г. с. с 1,15% С и 11,5% Мп видна из следующей таблицы (Rapatz): Зависимость механических свойств от условий нагрева и охлаждения для стали Гадфильдас 1,15% Си11,5%Мп.
Г. С. применяется исключительно в закаленном состоянии, в к-ром она, помимо высокой прочности и пластичности, обнаруживает большое сопротивление истиранию и износу. Из Г. с, готовятся изделия, работающие преимущественно на истирание, например ж.-д. стрелки и крестовины, болты и козырьки для землечерпалок, челюсти для камнедробилок, пробки для прокатки труб. Широкому распространению Г. с. препятствует трудность горячей ее обработки давлением и холодной обработки резанием; этим вызывается необходимость готовить изделия из нее путем отливки. (См. Справочник физ., шм. и технолог, величин, т. II.) Лит.: Бабошин А. Л., Металлография и термич. обработка железа, стали и чугуна, ч. III, П., 1917; Борнгэм Т. и Гадфильд Р., Специальные стали, Л., 1926; Mars G., Die Spezialstahle, 2 Aufl., Stuttgart, 1922; Rapatz F., Die Edel-stahle, Berlin, 1925 (имеется русский пер.); S с li a -fer R., Die Konstruktionsstahlc und Ihre warme-hehandluiig, Berlin. 1923. - M. Окиов. ГАЕЧНЫЙ КЛЮЧ, инструмент, служащий для отвинчивания и завинчивания гаек. Усилие Q, необходимое для завинчивания или отвинчивания гайки, приведенное к радиусу внешней окружности резьбы, выражается следуюпщм образом: П - Т>1г л. / + COSMga\ ~ Vd COSp-/-tgaj. где Р-нагрузка в кг на болт вдоль его оси, а-угол наклона средней винтовой линии резьбы к опорному торцу гайки, 2-угол при вершине треугольника, образующего остроугольный профиль нарезки, f-коэфф. трения между поверхностями резьбы у бол- /tr>v % vvtihf та и гайки, Д-коэфф. трения между гайкой и 4> 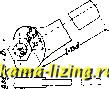 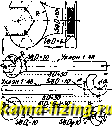 Фиг. 1. Фиг. 2. опорной поверхностью, 1>-наружный диаметр в см кольцев. площади торцевой опорной поверхности гайки, d-внутренний диаметр в см той нее поверхности, равный нарумсному диаметру болта. Момент, вы-зьшающий изгиб в челюстях и рукоят- ке ключа при его работе, 14= 4 Прочные размеры для Г. к, определяются расчетом на изгиб челюсти и рукоятки, Правильн, форма и размеры Г. к., по Баху, указаны на фиг. 1. Построение очертания челюстей и размеры американских гаечных ключей изображены на фиг. 2. Размер челюстей в направлении, перпендикулярн. к оси гайки в плоскости ее грани, выполняется или -addoiOi  Фиг. 4. равным d или более d на 3-5 мм. Изготовляют обычно Г. к, из литого железа штамповкой. Г, к. из ковкого чугша дешевле, но не так прочны, как штампованные. Поперечному сечению рукоятки гаечн. ключа часто придают двутавровую форму. Для гаек утопленных или располо-неенных так, что работать нормальным ключом не представляется возможным, употребляются торцевые ключи (фиг, 3); для круглых гаек, имеющих на боках высверленные углу-а!Х/\ бления или пропиленные - - пазы, применяется бель- Фиг. 5.  Фиг. 6. гийский ключ (фиг. 4); для круглых утопленных гаек применяется вильчатый ключ (фиг. 5). В тех случаях, когда желательно уменьшить толщину челюстей, Г. к, выполняют с замкнутым зевом (фиг, 6), Для того, чтобы можно было одним ключом завинчивать гаййи различных размеров, 1\ к, выполняют с раздвижными щеками; такие Г. к.  Фиг. 7. Фиг. 8, 9 и 10. называются универсальньши. Из многочисленных конструкций универсальных ключей наиболее совершенной является конструкция шведского ключа Бако (Bahco, фиг. 7); менее удобны для работы ключи- английский (фиг. 8), французский (фиг, 9) и швейцарский (фиг. 10), Лит.: Сидоров А, И., Курс деталей машин, 2изд.,ч. I, М.-Л.,1927; его те, Детали машин. Таблицы чертежей, М., 1925. Б. Шпрмин. ГАЗ. Газообразным состоянием называется такое состояние вещества, в к-ром силы, действующие между молекулами, чрезвычайно малы и размеры самих молекул ничтожны сравнительно с промежутками мелоду ними. Между столкновениями молекулы Г. двигаются прямолинейно, равномерно и совершенно беспорядочно. При нагревании и разрежении все Г. стремятся к предельному состоянию так называемого идеального, или с о в е р-ш е НПО го Г. В идеальном Г. междумолекулярные силы равны нулю, и объем самих молекул бесконечно мал сравнительно с объемом междумолекулярного пространства. Состояние идеального газа является-тем предельным разведенным состоянием вещества, к которому стремятся все тела природы при достаточно высоких t° и достаточно низких давлениях; в этом и заключается особое значение состояния идеального газа, к тому же наиболее просто поддающегося исследованию и потому полнее всего изученного. Вещество, в крайнем разрежении заполняющее межпланетное пространство, может считаться находящимся в состоянии идеального газа. Газовое давление р обусловливается ударами молекул Г. о стенки сосуда. Согласно кинетической теории (см.), средняя кинетич. энергия молекул Г. пропорциональна абсолютной темп-ре. В кинетическ. теории показывается, что идеальный газ строго подчиняется следующему уравнению состояния, связывающему три параметра состояния: v, 7и р, из к-рых два являются независимыми, а третий-их функцией: p-vRT. (1) Это ур-ие (ур-ие Клапейрона) заключает в себе в явной форме три основных закона состояния идеального Г.: 1) Закон Бойля-Мариотта. При постоянной Т произведение p-v для данного количества идеального газа есть величина постоянная (р-г- = Const), т. е. объем идеального газа v обратно пропорционален его давлению р: изотермы идеального газа в системе координат {v, р) -являются равнобокими гиперболами, асимптотами которых служат оси координат. 2) Закон Гей-Люссак а. При постоянном р объем данного количества идеального Г. линейно возрастает с t°: v = v{\+at) (2) (г?о-объем при Г = 0°С, -коэфф. расширения идеального Г.). Изменение р с t° при i;=Const подчиняется такому же закону: p=Poa + cc-t). (3) а в ур-ии (3)-коэфф. давления, численно равный коэфф. расширения к в ур-ии (2) = =-21-= 0,00367-величина, независящая от природы Г. и одинаковая для всех идеальных Г.; ро-давление при t° = 0°С. Вводя вместо t абсолютную темп-ру Г = -Ь =-Ь 273,1, находим вместо уравнений (2) и (3): v = T; (4) 273,1 273,1 Т. 3) ЗаконАвогадро. Из ур-ия (1) видно, что газовая постоянная R = 273,1 г; пр опорциональна нормальному объему Vq, занимаемому данным количеством Г. при нормальных условиях (Ро = 1 Atm и t = 0°C = 273,1° К), т. е. обратно пропорциональна плотности газа при нормальных условиях Do. По закону Авогадро, при одинаковых р я Т все идеальные газы содержат в равных объемах (напр., равных го) равное число молекул. Обратно: равное число молекул (например, 1 моль = 1 граммо-лекуле) всякого газа в идеальном состоянии занимает один и тот же объем Vg при нормальных условиях, независимо от природы Г. (в 1 моле всякого вещества содерясится Ац=6,06-103 отдельньЕХ молекул-число Авогадро). Найдено с большой точностью, что нормальный молярный объем любого идеального газа (Го) ра- вен 22,412 ; литр Отсюда можно рассчитать моль число молекул в 1 см любого идеального Г. при нормальных условиях: щ = = = 2,705-101 сл*з (число Лошмита). При помощи ур-ия (1) закон Авогадро выражается в том, что газовая постоянная R при расчете на 1 моль любого Г. будет одна и та же, независимо от природы Г. Т. о. В является универсальной постоянной с размерностью и выражает работу расширения 1 моля идеального Г. при нагревании его на 1°С при р = Const: в этом и состоит физическое значение R. 273,1 находим числовое значение R = - 22,416 - 0,082 литр атм. 273,1 моль град. В других единицах значения R моль) таковы: (на 1 i2=8,315-107: = 1,987 cal, 5 моль град. моль град. -Кроме разобранных трех законов, из уравнения (1) состояния идеального Г. в соединении с двум.я началами термодинамики следуют еще такие основные законы: 4) Закон Джоуля. Одно из общих ур-ий термодинамики (см.) дает вме сте с ур-ием (1) следующие условия для внутренней энергии U идеального Г.: \ др It т. е. z7 идеального газа есть функция только Т (закон Длоуля); при изотермич. расширении идеального газа все поглощаемое тепло переходит во внешнюю работу, а при изотермическом сжатии вся расходуемая работ-в выделяющезся тепло. 5) Теплоемкости идеального Г. при постоянном объеме и при постоянном давлении являются функциями одной лишь Т (см. Теплоемкость). Термодинайшка дает общие уравнения: Xdvl-p \дТ) Кдр/т ЛдТЧр но для идеального Г. р и w линейно зависят от Т, по закону Гей-Люссака (4) и (5); следовательно, правые части уравнений (9) обращаются в О и Теплоемкости Ср и не независимы друг от Друга, но связаны для идеального Г. простым условием: Ср-с, = М, (10) вытекающим из газовых законов (R имеет размерность теплоемкости), т. е., если Ср и относить к 1 молю идеального Г., то они разнятся между собой на 2 (точнее-на 1,986) calls моль град. В кинетической теории принтхается, по принципу равномерн. распределетшя энергии, что на каждую степень свободы газовой молекулы приходится энергия JcqT, а на 1 моль приходится (ко= - есть газовая постоянная, рассчи- тайная на 1 молекулу - постоянная Больцмана). Числом степеней свободы (г) называется число независимых друг от друга видов механич. энергии, которой обладает молекула Г. Тогда энергия 1 моля U=-i.R-T и = (11) cc + R=[i+l). R (12) (приближенно, считая i2=2, %=г, Cp=i-\-%). В учении о Г. важную роль играет отношение = у; из уравнений (11) и (12): У=1 + --Г (13) в простейшем случае одноатомного Г. (молекула к-рого состоит из 1 атома, каковы благородные Г. и пары многих металлов) i наименьшее и равняется 3: вся энергия молекулы сводится к кинетич. энергии ее поступательных движений, которые могут совершаться по трем независимым взаимно перпендикулярным направлениям; тогда =2,983, 0=4,985, , а у имеет наибольшую возможную величину: 7 = = 1,667. Для двухатомных Г. (На, Оз, Ng, СО и другие) можно считать г = 3-Ь2 (два вращения вокруг двух взаимно перпендикулярных осей, перпендикулярных к линии, соединяющей оба атома); тогда с = 4,96 5, Ср = 6,95 7 и у = - = 1,40. Для трехатомного Г. (HjO, СО2, HS, N20)1 = 3 -Ь 3 (вращение вокруг трех взаимно перпендикулярных осей) и с =5,966, Ср=7,958 и у = -1=1,33. При дальнейшем усложнении строения молекулы, т. е. с увеличением г, возрастают си Ср, а 7 = 1 -f -- и стремится к 1. Табл. 1 показывает, что все сказанное хорошо согласуется с данньши опыта, что у всегда >1 и 1,667 и не может быть = 1,50 (для г=4). Табл. 1. - Экспериментальные значения Ср, сриу для газов.
Для одноатомных Г. и Ср, в соответствии с теорией, практически не изменяются с Т (так, для Аг значения с и Ср лежат в пределах от 2,98 до 3,00 между t° = 0° и 1 000° С). Изменения с,;И Ср с Г находят объ-.яснение в теории квант. Впрочем, теплоемкости Г., близких к идеальным, практически почти не изменяются в широких интервалах температуры. Экспериментально определяются обычно Ср и у, а вычисляется из этих данных. Реальные Г. Все Г., существующие в действительности,-рсальные Г. б. или м. уклоняются от законов идеальных Г., но тем меньше, чем выше t° и чем ниже р. Т.о. законы идеальных газов являются для реальных газов предельными. При обычной t° уклонения меньше всего у Г., t\pum. к-рых чрезвычайно низки (т. н. постоянные газы: Не, Hg, Ng, Oj, воздух); у газов же со сравнительно высокой i°wpum. и у паров (паром назьшается Г. при t°< t%pum.) уклонения бывают очень значительны. Причины уклонений реальных Г. от газовых законов заключаются в том, что: 1) в них действуют междумолекулярные силы; поэтому поверхности, молекулы втягиваются внутрь газов силами, равнодействующая которых, рассчитанная на единицу поверхности и направленная перпендикулярно к ней, называется молекулярным (внутренним) давлением К; 2) не весь объем Г. г;, а только часть его (v-b) дает свободу для движений молекул; часть объема Ъ, к о в о л ю м, как бы занята самими молекулами. Если бы газ был идеальным, его давление было бы больше наблюдаемого р на величину К; поэтому уравнение состояния реального Г. напишется в виде. (p+K)-(v-b)=R Т. (14) В этом общем уравнении К и b могут зависеть от Т и V. Ван-дер-Ваальс показал,что в простейшем случае К = ~, а b-величина постоянная, равная учетверенному объему самих молекул Г. Таким образом уравнение Ван-дер-Ваальса имеет вид: [p+)-{v-b)=TR; (15) а и Ъ, константы Ван-дер-Ваальса, как ноказьшает опыт, все же зависят от Т и г;, и потому ур-ие (15) является лишь первым приближением; оно хорошо передает качественную форму изотерм реальных Г. На фиг. 1 изображены для СО2 теоретич.
|
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||