
 |
|
|
Литература --> Доменное производство металла едкие щелочи диссоциируют на ионы металла и гидроксильные ионы, например: кон К + ОН Ва(0Н)2 : (ВаОН) + ОН (ВаОН)Ва + ОН По классической теории, степень диссоциации (см. Диссоциация электролитическая) различных едких щелочей (при 18°) составляет (в %): LiOH в Vi N растворе...........63 NaOH N ...........тз КОН Vi N ...........77 Са(0И)2 VeiN ...........90 Sr(OH), U,N ..........-92 Ва(ОНЬ UtN ...........93 Е. щ. являются, Т. О., сильными основаниями, при чем щелочный характер (как и растворимость) возрастает с увеличением ат. в. Растворы Е. щ. хорощо проводят электрич. ток, что связано с большой подвижностью иона ОН. По современной теории Е. щ., как сильные электролиты, д. б. полностью диссоциированы на ионы. В согласии с этим находится и результат исследования Е. щ. в твердом состоянии с помощью рентгеновских лучей, показывающий, что кристаллы этих веществ построены из ионов и обладают ионной решеткой (см. Кристаллы). Лит.: GmeUn и. Krauts Handbuch der anorgani-schen Chemie, Heidelberg, 7 Aufl., 1905-16, 8 Aufl., ab 1924; Arrhenius S., Theorien d. Chemie, 2 Aufl., В., 1909; Ostwald W., Grundlinien d. anorgan. Chemie, 5 Aufl.. Dresden-Lpz., 1922; L a nd 0 1 t-B б r n s t e i n. Physikalisch-chemische Tabel-len. 5 Auflage, B. 1-2. В., 1923. И. Казарновский. ЕДКИЙ НАТР, NaOH, гидрат окиси натрия, каустическая сода, белая непрозрачная масса с волокнистым изломом, уд. в. 2,0-2,13, плавящаяся в безводном состоянии при 318°, t°K n 1388°; Е. н. легко растворяется в воде с значительным выделением тепла, давая сильно щелочи. раствор.Теплота образования NaOH из элементов-101,9, а в растворе 111,8 Cal. Для теплоты растворения в 200 молях воды Томсен нашст величину -Ь9,9, а Вертело (в 135-154 молях при 10,5°) + 9,8 Cal. Теплота образования моногидрата из безводного NaOH равна 3,25 Cal; удельная теплоемкость NaOH мелсду О и 98°-0,78. В растворе диссоциировано на ионы бо-.лее 70% NaOH, а в Vio растворе-ок. 90%. Существует несколько гидратов Е. п.: с 1, 2 и 3,5 молекулами HgO (их t%,, соответственно: 64,3, 12,7 и 15,6°). Во влалшом воздухе Е. н. расплывается, но в присутствии углекислоты быстро покрывается белой коркой соды, и расплывание прекращается (отличие от едкого кали). Растворы Е. и. уже давно приготовляли кустарным путем для целей мыловарения, но первая попытка заводского производства была сделана лишь в 1844 году в Англии. С 1890 г. начинает применяться электролитический метод. Для получения Е. н. можно исходить или из маточных растворов, остающихся при производстве соды по способу Леблана после выделения главной массы соды, т. е. из т. п. красного щелока, или же из содового плава, изменив пропорции при его получении, т. е. увеличив количество угля. П.лав выщелачивают водой при 50° и выпаривают раствор, при чем выделяются сода, сернокислый и хлористый нат- рий, и жидкость приобретает кирпично-крас-ный цвет (вследствие образования двойного соединения сернистого натрия с сернистым железом). Отделенный от солей щелок, содержащий также и цианистый натрий, продолжают сгущать. Для разрушения примесей через раствор продувают воздух (при этом происходит окисление NagS в NagSaOg) и нри более высокой t° прибавляют малыми порциями селитру; цианистый натрий разлагается с выделением аммиака, железо осаждается, сернистые соединения окончательно окисляются. Освобожденный от солей (путем вычерпывания их) и осветленный щелок с уд. в. 1,5 переводят в плавильный котел. Общеизвестным и наиболее распространенным способом получения Е. н. является взаимодействие раствора соды с известковым молоком (известковый способ): N3003 +Са(0П)г : 2NaOH + CaCO,. Выход Е. и. тем больше, чем слабее раствор соды, но в технике предпочитают пользоваться 10-12%-ным раствором соды. Реакцию ве)1;ут в железных цилиндрах, снабженных мешалками, нагревая раствор в течение 1-IV2 часов паром до кипения. Высокая t° только ускоряет течение процесса, но не изменяет существенно выхода. Увеличение давления не сказывается на результате. Для реакции пользуются обыкновенно аммиачной содой, как более чистой. Для фильтрования растворов пользуются или фильтр-прессами или вращающимися н у ч а м и. Последние имеют вид барабанов, обтянутых фильтрующей тканью, а поверх нее-дырчатыми железными листами. Такой цилиндр медленно вращается вокруг горизонтальной оси в корыте,нанолненном фильтруемой жидкостью. Радиальными перегородками он разделен на ряд камер, соединенных с отсасывающими насосами. Жидкость засасывается в эти камеры, откуда поступает в сборные чаны, а осадок остается на поверхности цилиндра. Содержащийся в нем NaOH промывают струей воды, после чего осадок удаляют скребком. Щелок, получающийся при работе по известковому способу, содернгит 10-12% NaOH. Из других химическ. способов получения Е. п. можно упомянуть еще о способе Лё-вига (Г. П. 2i593), предложенном в 1882 г. По этому способу, возможно более чистую соду прокаливают с чистой окисью железа, свободной от кремнезема и глинозема, в муфельных или револьверных печах при ярко-красном калении. Происходит выделение углекислоты и образование феррита натрия: NajCO. + FCjO, = Na.FcaO. + CO j. Последний, представляющий собой крупнозернистый зеленоватый порошок, разлагается горячей водой на NaOH и окись железа, к-рая снова поступает в производство: NajFeO, + НО = 2 NaOH + FCaO,. Предварительно извлекают холодной водой легко растворимые соли: NajCOg, NaCl. Получаемый щелок очень чист; содержание NaOH достигает в нем 25-30%. Хотя такие крепкие растворы требуют для выпаривания меньше топлива сравнительно с растворами, получающимися при известковом способе , но в общем расход топлива при работе по способу Лёвига оказывается выше. Больше всего примесей содерясит технич. Е. п., полученный из соды, приготовленной по способу Леблана. Электролитически Е. п. получается из раствора хлористого натрия по уравнению: 2 NaCl + 2 HsO = 2 NaOH + Н + Clj. Как ни проста эта реакция, однако, практич. осуществление ее уже в первых стадиях встречает ряд затруднений: освобождающийся хлор легко реагирует со щелочью, давая ряд побочных продуктов (соли хлорноватистой и хлорноватой к-т). Во избеяеание этого растворы, находящиеся у катода и у анода, предохраняются от взаимного смешения, например, путем установки в ванне диафрагмы. Диафрагма д. б. устойчивой к хлору и щелочи, достаточно проницаемой и недорогой. Образовавшаяся щелочь такясе принимает участие в электролизе, при чем к аноду передвигаются ионы ОН, обладающие наибольшей подвижностью из всех анионов. При комнатной t° и при падении потенциала в 0,1 V на 1 см, подвижность их составляет 0,0018 мм/ек, или 6,48 лгл/ч. Реагируя с растворенным в жидкости хлором, ионы ОН будут давать ионы хлорноватистой кислоты; 2 ОН + CU СЮ + сг + н,о. Кроме того, и элементарный хлор реагирует у анода с водой по ур-ию: С1а + що 1; н- + сг + Н + осг. Разряжение ионов СЮ сопровождается образованием кислорода, примешивающегося к хлору, и ионов хлорноватой к-ты: 6C10 + 3HsO бН* + 2С10з + 4СГ + 30. Кислорода образуется тем больше, чем слабее раствор соли. Поэтому необходимо работать с концентрированными растворами. Кислород моясет образовываться на аноде и ири разряжении анионов SO4, если в техническом NaCl присутствует примесь сернокислых солей. Поэтому нужно заботиться о том, чтобы в исходной поваренной соли их было возможно меньше. Очень серьезным является вопрос о материале электродов, особенно анода, у к-рого выделяется хлор. Раньше аноды изготовлялись из размолотого кокса или ретортного угля с прибавлением смол и последующим обжиганием их. Отличаясь устойчивостью по отношению к хлору, они окисляются кислородом в момент его выделения, и т. о. к хлору примешивается углекислота. При значительном ее содержании (до 10%) хлор становится уже непригодным для получения хорошей белильной извести. Вообще, чем более порист уго.ть, тем быстрее он разрушается. Значительно устойчивее аноды из графита Ачесо-на, изготовляемые в Америке, а в настоящее время и в Германии. Совершенно не образуется СО 2 ири магнетитовых анодах из сплавленной при t° 2 ООО-3 000° закиси-окиси железа Рез04 (Г. П. Грисгейм-элек-трон 157122 и 193367). Они проводят ток несколько хуясе, чем угольные аноды, и требуют поэтому большего напряягения (4,05- 4,1V вместо обычных 3,65 V). Зато они очень прочны, служат по 5-7 лет и по нерастворимости не уступают платине. Материалом для катодов служит обычно железо. Правда, оно не вполне устойчиво в щелочной среде и разъедается в концентрированных растворах соли (особенно в присутствии хлоратов), но зато на ясе.лезе в щелочной среде водород очень легко выделяется (разряжается), а, кроме того, железо дешево, почему его и предпочитают никелю и меди. Способы элеьстролитич. получения едких щелочей м. б. сведены к 3 тинам. Отличительными признаками их являются: 1) твердые катоды и диафрагмы, 2) твердые катоды без диафрагм (с применением колокола) и 3)жидкие катоды (ртутный способ). I тип (с применением диафрагмы). Элек-тролитич. производство едких щелочей впервые было осуществлено в технич. масштабе на з-де в Грисгейме в 1890 г., после того как удалось приготовить надлеясащую диафрагму из цемента на растворе поваренной соли (Г. П. 34888). После затвердевания цемента соль выщелачивается водой, благодаря чему получается очень мелкопористая прочная пластина. Было предложено много различных диафрагл! (состоящих обыкновенно из асбеста или асбеста с цементом и т. п.) и различных видоизменений первоначального способа. Способ, принятый в Грисгейме, состоит в следующем. Ряд железных ванн площадью 5хЗ,5ж2, содерясащих каждая по 12 ячеек, соединены последовательно группами по 30 шт. (ячейки каждой ванны включены параллельно). Каждаятакая группа питается постоянным током от динамо-машины в 110 V при 2 500 А, так что на каждую ванну приходится в среднем напряжение в 3,65 V; ири большей силе тока напряжение-выше. На фиг. 1 показаны ячейки в вертикальном разрезе. В каждой ячейке находится продолговатый оцементи-рованный ящик J) площадью в 1,1 X0,75 лг и высотой в 1 Л1. В боковых стенках каждого ящика вставлено 6 пористых цементных диафрагм (по две на длинных и по одной на узких сторонах ящика). Против диафрагм в каждом ящике подвешены 6 толстых угольных анодов А, которые присоединены к одному общему проводнику. Посредине помещается глиняный сосуд t с отверстиями, нанолнен-ный твердой солью, периодически добавляемой. Снаружи ящиков (в катодном отделении) укреплены железные пластины К, соединенные со стенками ванны и служащие катодами. Анодное и катодное отделения закрыты крышками, через к-рые выходят трубы а VL h для отвода хлора и водорода. Ванну наполняют крепким раствором соли, который нагревают до 80-90°; нагревание ведется при помощи паровой трубы w. Когда разлоясится ок. соли, катодный раствор, содержащий 60-80 г NaOH (или 80-110 г КОН) на л, выпускают из ванны и подвергают выпариванию, ванну же наполняют свеясим раствором. По мере увеличения количества щелочи в ягидкости ионы ОН принимают все большее и большее участие в 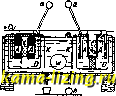 Фиг. 1. переносе электричества, и на аноде начинает выделяться не более 80-85% теоретич. количества щелочи и хлора. Уменьшение выходов хлора и щелочи, обусловливаемое передвижением гидроксильных ионов к аноду, пытались парализовать (напр. в способе Гар-гривс-Бёрда, Нельсона) тем, что раствор заставляли непрерывно протекать в обратном направлении (от анода к катоду) при вертикальном положенпи диафрагм. Впоследствии были предложены горизонтальные диафрагмы. Одним из лучших и довольно распространенных способов I типа в настоящее время является способ Биллитера (Г. П. 191234 и 254780), разработанный им совместно с фирмой Сименс и Гальске. Аппарат Биллитера снабжен горизонтальной диафрагмой, и в нем имеется постоянное движение раствора соли от анода к катоду. Продольный и поперечный разрезы аппарата приведены на фиг. 2 и 3. Аппарат состоит из колокола 11, закрытого снизу диафрагмой 2, покрывающей железную или никелевую сетку 5, слулащую катодом. Колокол окружен  Фиг. 2. Фиг. 3. сосудом 10. Внутри колокола находится анод 8 из платины, угля или магнетита, расположенный параллельно катоду и на небольшом от пего расстоянии. Колокол наполняется до известной высоты электролитом, а сосуд 10 остается временно пустым, Т, к. диафрагма проницаема для жидкостей, то раствор соли проникает через нее к катоду, где образуется NaOH; 13-выходное отверстие для щелочи. Свежий раствор притекает через трубку 12, оканчивающуюся недалеко от диафрагмы. Во время электролиза уд. вес верхней части раствора уменьшается, так как она беднеет солью, а уд. в. нижней части увеличивается. Т. о., неносредственно над диафрагмой образуется довольно резкая поверхность раздела. Если к КОЛОКО.ТУ присоединить камеру 9 из не-пропицаемого материала, наполненную твердой солью, так, чтобы слой, непосредственно прилегающий к диафрагме, постоянно насыщался ею, то уд. в. его еще более увеличится. В сосуде 10 помещена еще перегородка 5, через к-рую должен перетекать раствор, так что он омывает катод также и с нижней стороны. Благодаря этому приспособлению удаляются даже незначительные количества NaOH, продиффундировавшего в колокол, т. к. переливаться через перегородку должен именно самый пилений слой, непосредственно прилегающий к диафрагме. (Для большей наглядности расстояние между 5 и 11 на чертенке несколько преувеличено; в действительности же оно очень невелико.) Диафрагмой 2 служит паста из асбеста и сернокислого бария, к-рая накладывается слоем на асбестовое полотно 1, покрываю- щее катод; паста эта приготовляется осаждением сернокислого бария с мелким асбестом из 20%-ного раствора новаренной соли; ее легко высушивать, придавая любую форму, к-рую она сохраняет далее при продолжительном нахождении в жидкой среде. Такие диафрагмы очень прочны и в случае надобности могут быть легко сменены. Вследствие-своей гибкости диафрагма плотно прилегает к катоду и не отстает от него при выделении водорода; т. о., равномерность процесса не нарушается. Варьируя количество асбеста и тялеелого шпата, можно по лселанию изменять пропускную способность диафрагмы. Для облегчения выхода водорода ей придают б. ч. не горизонтальную, а волнообразную поверхность. В зависимости от силы тока нанрянеение в ваннах составляет 3,5-4 V, утилизация тока-до 95%. Аппарат дает 12-16%-ный раствор NaOHn 18-20%-пый раствор КОН. Способ Биллитера требует меньше электрич. энергии, чем способ Гри-сгейм-электрон, и, кроме того, на 30-40% меньше топ.пива на выпарку щелочных растворов, т. к. они получаются более крепкими. Биллитер предложил еще один способ, не описанный пока подробно в литературе и характеризующийся присутствием стеклянной диафрагмы (из стеклянной ваты, пропитанной силикатом) с вертикальными анодами. Вообще, как показал опыт, вертикальное расположение анодов является очень удобным; ваннам такого тина теперь уделяется много внимания. II тип (с применением колокола). Принцип этого способа (Г. П. 141187) молшо видеть из помещенного ншке схематич. чертежа (фиг. 4). В ванне W находится колокол G из непроводящего материала с анодом А; катодом служит К, по трубке L поступает раствор соли, через С выходит хлор, а через F вытекает щелочной раствор. В практике употребляются узкие, прямоугольные, закрытые сверху железные ящики (колокола), размером приблизительно 150 X 30 X (154-20) см, покрытые внутри толстым изолирующим слоем (фиг. 5). В них находятся угольные аноды А. Раствор соли поступает через канал В и трубку С, которая имеет сверху ряд отверстий, обеспечивающих равномерное и спокойное поступление электролита. Через трубку D выделяется хлор. Отверстия Е служат для скрепления смежных колоколов. На фиг. 5 представлен продольный и поперечный разрез отдельного колокола. Работа ведется при темп-ре не выше 35°. Сила тока не должна превышать 30 А на колокол. На з-де в Ауссиге, потребляющем 2 ООО-3 ООО ЬР, таких колоколов д. б. до 25 ООО шт. При утилизации тока в 85- 90% и при напрял-сении в 4-5 V получается раствор с содержанием 100-150 г едких щелочей в л. Недостатком описанного 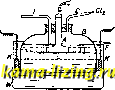 Фиг. 4. Фиг. 5.
|